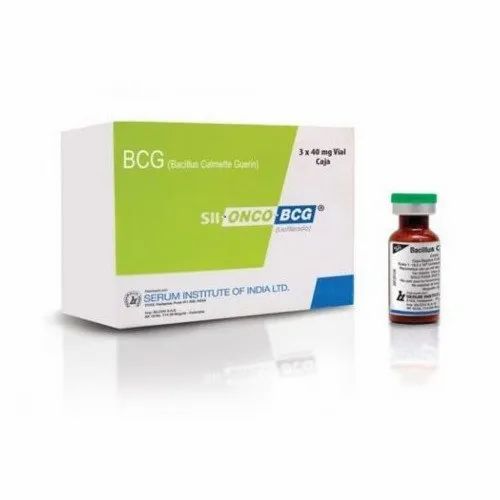
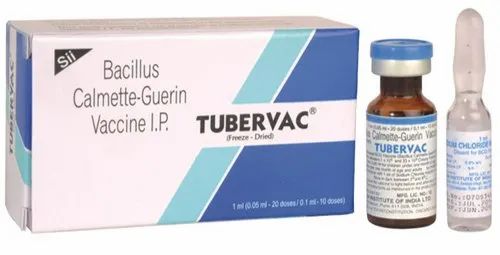
BCG {Bacillus Calmette-Guerin} Vaccine
Si Disponible: Dispensado al Día Siguiente
Envío Gratis
Dentro de México
Requiere Receta Médica
Este Medicamento requiere prescripción médica de su médico, clínica, hospital o terapeuta.
BCG Onco Vaccine / Vacuna BCG
Clase:
Vacunas contra el virus BCG.
Cómo Suministra:Instilación Intravesical
(liofilizado)
Description
BCG Vaccine (Bacillus Calmette–Guérin)
Live Attenuated Vaccine – Tuberculosis Prevention
WHO Prequalified | Indian DCGI Approved | Prescription Only
Product Description:
BCG (Bacillus Calmette–Guérin) Vaccine is a live attenuated vaccine derived from Mycobacterium bovis and is used for active immunization against tuberculosis (TB). It provides protection primarily against severe forms of TB such as miliary TB and TB meningitis in infants and young children.
The vaccine contains a freeze-dried preparation of the attenuated strain of Mycobacterium bovis and is reconstituted with a sterile diluent prior to intradermal administration. Products manufactured by Serum Institute of India Pvt. Ltd. and Cipla Ltd. are WHO-GMP compliant, with selected batches WHO-prequalified for international procurement.
Available Presentations:
- Strength: Each vial contains sufficient BCG vaccine for:
- 10-dose vial: Reconstituted with 1 mL sterile diluent
- 20-dose vial: Reconstituted with 2 mL sterile diluent
- Formulation: Freeze-dried (lyophilized) vaccine
- Packaging: Glass vial + ampoule of diluent in single carton
- Route of Administration: Intradermal (typically in left deltoid area)
- Storage Conditions: 2°C to 8°C; protect from light; do not freeze
Uses:
- Active immunization against tuberculosis, especially:
- Miliary TB
- Tuberculous meningitis
- Administered in:
- National childhood immunization programs
- WHO Expanded Programme on Immunization (EPI)
- Hospitals, neonatal wards, and humanitarian aid settings
Indications:
- Neonatal and infant immunization in TB-endemic regions
- WHO-recommended for:
- Newborns in countries with high TB incidence
- Immunization within first 24 hours of life where possible
- May be used in occupational or high-risk adult populations under clinical guidance
Regulatory and Safety Profile:
- Manufacturers: Serum Institute of India Pvt. Ltd., Cipla Ltd.
- Regulatory Approvals: WHO Prequalified (select lots), DCGI Approved, WHO-GMP Certified
- Pregnancy Category: Contraindicated
- Common Adverse Effects: Local injection site reaction, ulceration, regional lymphadenitis
- Serious Risks: Disseminated BCG disease in immunocompromised infants
- Contraindications:
- Known or suspected immunodeficiency (e.g., HIV-exposed infants)
- Febrile illness or symptomatic infection at time of vaccination
- Monitoring: Local skin reaction, lymph node swelling, immune status if HIV risk suspected
For pricing, batch availability, COA requests, and cold-chain shipment inquiries, please contact info@panamfarma.com.