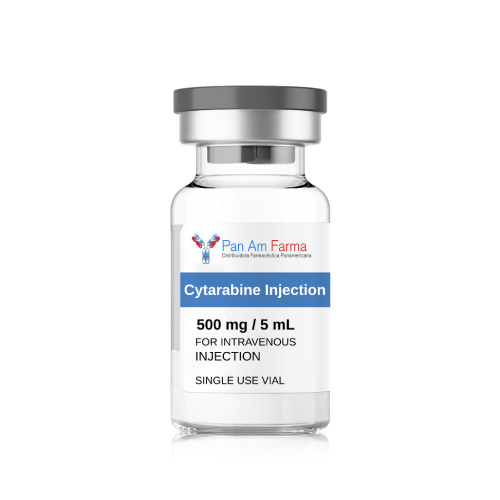
Cytarabine 500mg / Citarabina 500mg
Si Disponible: Dispensado al Día Siguiente
Envío Gratis
Dentro de México
Requiere Receta Médica
Este Medicamento requiere prescripción médica de su médico, clínica, hospital o terapeuta.
Cytarabine / Citarabina
DESCRIPCIÓN:
Cytarabine is a chemotherapy medication used to treat certain types of leukemia by inhibiting the growth of cancer cells.
Agente anitneoplásico antimetabolito de pirimidina; Citarabina está indicada principalmente para la inducción y mantenimiento de la remisión de leucemias agudas linfoblásticas y mieloblásticas, en adultos y niños; linfoma linfoblástico, fase blástica de la leucemia granulocítica crónica, meningitis carcinomatosa, linfomatosa o leucémica.
Description
Cytarabine / Citarabina 500mg
Clinical Utilization / Utilización Clínica
Cytarabine is an antimetabolite chemotherapeutic agent used primarily for hematological malignancies including AML, ALL, and CML by inhibiting DNA synthesis. La citarabina es un agente quimioterapéutico antimetabolito utilizado principalmente en el tratamiento de neoplasias hematológicas como LMA, LLA y LMC, inhibiendo la síntesis de ADN.Formulations / Formas y Presentaciones
- Injection, Solution: 500 mg/25 mL (20 mg/mL) multiple-dose vial for IV, SC, or intrathecal use.
- Inyección, Solución: Vial multidosis de 500 mg/25 mL (20 mg/mL) para uso IV, SC o intratecal.
NDC Codes / Números NDC
USA NDC: 61703-304-36Pricing / Precios
~$100 USD per 500 mg vial (may vary by region and supplier).~$100 USD por vial de 500 mg (puede variar según proveedor y región).
Concise Description / Descripción Comercial
Cytarabine is used in the treatment of leukemias by preventing cancer cell growth. Administered under medical supervision. La citarabina trata tipos de leucemia al impedir la proliferación de células cancerosas. Requiere supervisión médica.Mechanism of Action / Mecanismo de Acción
Cytarabine is S-phase specific and inhibits DNA polymerase after conversion to Ara-CTP. This halts DNA elongation and repair, particularly during maximal DNA synthesis. La citarabina actúa en fase S, inhibiendo la ADN polimerasa como Ara-CTP, deteniendo la síntesis y reparación del ADN, afectando especialmente a células en proliferación activa.Pharmacokinetics / Farmacocinética
- Routes: IV, SC, Intrathecal
- Not orally bioavailable (extensive GI deamination)
- CSF penetration: 20–50% of plasma levels
- Metabolized by cytidine deaminase; eliminated mainly via urine as Ara-U
- Terminal half-life: 1–3 hours (IV), 2–11 hours (CSF)
- Vías: IV, SC, intratecal
- No se administra oralmente (desaminación GI)
- Penetra LCR: 20–50% de niveles plasmáticos
- Metabolismo hepático, excreción renal como Ara-U
- Vida media terminal: 1–3 h (IV), 2–11 h (LCR)
Indications / Indicaciones
Used in AML (induction/postinduction), ALL, CML (chronic/blast phase), CNS leukemia, Hodgkin/NHL relapse, and conditioning for transplants. Indicada en LMA (inducción/postinducción), LLA, LMC (fase crónica/blástica), meningitis carcinomatosa, linfomas recidivantes, y acondicionamiento para trasplantes.Disclaimer / Aviso Legal: The products and information on this website are for informational and educational purposes only. Los artículos y la información de productos en este sitio web son únicamente con fines informativos y educativos.
*Not all products are approved by COFEPRIS, FDA, EMA, MHRA, or WHO for clinical use. Some may be for "In-Vitro" research only. *No todos los productos han sido aprobados por COFEPRIS, FDA, EMA, MHRA o WHO. Algunos son únicamente para estudios “In-Vitro”.